南昌去哪里能看白癜风-白癜风临床试验受试者招募
2026-03-05 11:21:57 来源: 南昌白癜风医院 咨询医生
尊敬的白癜风病友及家属:
您好!
本院皮肤科目前正在开展一项关于“磷酸芦可替尼乳膏”的临床研究。该研究旨在评估这一药物用于治疗非节段型白癜风的安全性和有效性,并已获得本院伦理委员会的正式批准。
研究背景与目的
白癜风是一种获得性、特发性色素脱失性疾病,其主要病理特征为皮肤黑素细胞功能丧失,导致皮肤出现局限性或泛发性白斑。流行病学数据显示,我国人群患病率约为0.1%-2%,且近年来呈现年轻化趋势。非节段型白癜风(包括散发型、泛发型、面肢端型及混合型)是常见的临床亚型,因其皮损范围广泛、影响美观,常给患者带来沉重的心理负担和社会交往障碍,严重影响生活质量。
目前白癜风的传统治疗手段主要包括外用糖皮质激素、钙调磷酸酶抑制剂、光疗(窄谱中波紫外线NB-UVB、308nm准分子光)及外科移植等。然而,传统疗法存在一定局限性:长期使用糖皮质激素易导致皮肤萎缩、毛细血管扩张等不良反应;光疗则需要患者频繁往返医院,治疗周期长,依从性面临挑战;对于稳定期患者的外科治疗,也存在适用人群有限、操作复杂等问题。因此,临床上亟需一种更加安全、便捷、有效的治疗选择。
近年来,随着对白癜风发病机制研究的深入,JAK-STAT信号通路在白癜风发病中的作用日益明确。研究表明,干扰素-γ(IFN-γ)及其诱导的趋化因子(CXCL9、CXCL10)在白癜风皮损局部高表达,通过JAK1/JAK2信号通路介导CD8+细胞毒性T淋巴细胞向表皮迁移,从而直接攻击黑素细胞,导致色素脱失。JAK抑制剂通过阻断这一信号通路,能够有效抑制免疫细胞向皮损处浸润,为黑素细胞的再生和迁移创造有利的免疫微环境。
本次临床研究的主要目的包括:
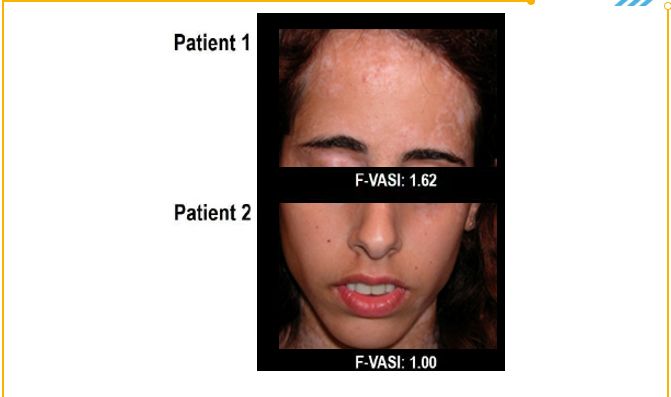
有效性评估:评估JAK抑制剂外用乳膏治疗非节段型白癜风24周及52周时,面部及全身皮损复色的改善程度,主要观察指标为面部白癜风面积评分指数(F-VASI)较基线的变化率,以及达到F-VASI 50、F-VASI 75(即面部白斑面积改善50%、75%以上)的患者比例;
安全性评估:观察研究药物在真实世界临床应用中,不同年龄段、不同病程、不同皮损部位患者中的安全性特征,包括不良事件发生率、局部耐受性及实验室指标变化;
生活质量影响评估:通过标准化生活质量问卷(如DLQI、Skindex-16等),评估治疗后患者心理状态、社交功能及生活质量的改善情况;
长期疗效观察:通过延长随访期,观察达到复色效果的受试者在停药后色素维持情况,为临床制定个体化治疗方案提供数据支持。
本研究的开展,将为中国白癜风患者提供更多的循证医学证据,进一步验证JAK抑制剂外用制剂在中国人群中的疗效和安全性特征,为优化临床治疗策略、实现精准治疗奠定基础。
入选标准
如果您或您的亲友符合以下基本条件,可能有机会参与本次研究:
• 年龄要求:年龄≥12周岁,性别不限;
• 诊断标准:临床确诊为非节段型白癜风(包括进展期或稳定期);
• 全身受累体表面积(BSA)介于10%以内;
• 面部受累BSA≥0.5%,且面部白癜风面积评分指数(F-VASI)≥0.5;
• 治疗意愿:自愿停止使用可能影响研究结果的其他白癜风治疗方案(以医生制定的治疗方案为准),并同意在整个研究期间仅使用研究指定的治疗方案;
• 知情同意:充分了解本研究内容,自愿签署书面知情同意书,并能配合完成定期的随访和检查。
排除标准
具有以下任一情况者,不宜参加本研究:
• 诊断为节段型白癜风或其他非节段型白癜风以外的色素减退性疾病(如无色素性痣、炎症后色素减退等);
• 筛选期存在活动性炎症性皮肤病(如湿疹、银屑病等),经研究者判断可能干扰疗效评估;
• 既往使用过皮肤脱色剂治疗;
• 伴有进展性或未控制的严重系统性疾病(如心脑血管疾病、恶性肿瘤、严重感染、免疫缺陷等);
• 妊娠期、哺乳期女性,或研究期间有生育计划且不愿采取高效避孕措施者;
• 已知对研究药物或其辅料成分过敏。
可能的风险与受益
潜在受益:参加本研究的受试者,有可能从治疗中获得皮损复色的效果。根据境外III期临床研究及中国真实世界数据,每日两次使用研究药物治疗24周后,有相当比例的患者面部白斑面积获得显著改善,且随治疗时间延长,复色效果持续改善。
潜在风险:研究药物可能引起局部不良反应,如用药部位的痤疮、瘙痒、红斑或刺激感。在已完成的临床试验中,不良反应的严重程度大部分均为1级或2级,未发生与药物相关的严重不良事件(SAE)报告。研究期间,您的病情将由专业医疗团队密切监测,一旦出现不适,将及时得到处理。
其他权益:
01 您将获得免费体检;
02 您将获得相应的医疗补助;
03 您的个人信息是保密的,您的权益将会得到保障。
报名方式
本研究计划招募100名受试者。
如果您符合上述条件,并希望了解更多信息,请通过以下方式联系我们:
招募专线:15170099064
招募期限:即日起至招满为止。
特别提示:本信息发布目的为招募临床试验受试者,不构成任何用药建议或广告宣传。是否入选将由研究医生根据详细的入选/排除标准评估后确定。
附:客观数据支撑
国际III期研究(TRuE-V1/V2):治疗24周时,面部白斑面积改善≥75%(F-VASI 75)的患者比例达到29.9%(安慰剂组为7.5%-12.9%)。
中国真实世界研究:使用24周后,达到F-VASI 75的患者比例为49.5%,疗效积极。
安全性数据:长期使用至52周,未发现新的安全性事件。
您好!
本院皮肤科目前正在开展一项关于“磷酸芦可替尼乳膏”的临床研究。该研究旨在评估这一药物用于治疗非节段型白癜风的安全性和有效性,并已获得本院伦理委员会的正式批准。
本研究严格遵循《药物临床试验质量管理规范》(GCP)及赫尔辛基宣言,所有招募流程均以医疗科研为目的,现面向社会公开招募受试者。
研究背景与目的
白癜风是一种获得性、特发性色素脱失性疾病,其主要病理特征为皮肤黑素细胞功能丧失,导致皮肤出现局限性或泛发性白斑。流行病学数据显示,我国人群患病率约为0.1%-2%,且近年来呈现年轻化趋势。非节段型白癜风(包括散发型、泛发型、面肢端型及混合型)是常见的临床亚型,因其皮损范围广泛、影响美观,常给患者带来沉重的心理负担和社会交往障碍,严重影响生活质量。
目前白癜风的传统治疗手段主要包括外用糖皮质激素、钙调磷酸酶抑制剂、光疗(窄谱中波紫外线NB-UVB、308nm准分子光)及外科移植等。然而,传统疗法存在一定局限性:长期使用糖皮质激素易导致皮肤萎缩、毛细血管扩张等不良反应;光疗则需要患者频繁往返医院,治疗周期长,依从性面临挑战;对于稳定期患者的外科治疗,也存在适用人群有限、操作复杂等问题。因此,临床上亟需一种更加安全、便捷、有效的治疗选择。
近年来,随着对白癜风发病机制研究的深入,JAK-STAT信号通路在白癜风发病中的作用日益明确。研究表明,干扰素-γ(IFN-γ)及其诱导的趋化因子(CXCL9、CXCL10)在白癜风皮损局部高表达,通过JAK1/JAK2信号通路介导CD8+细胞毒性T淋巴细胞向表皮迁移,从而直接攻击黑素细胞,导致色素脱失。JAK抑制剂通过阻断这一信号通路,能够有效抑制免疫细胞向皮损处浸润,为黑素细胞的再生和迁移创造有利的免疫微环境。
本研究涉及的研究药物是一种JAK1/JAK2抑制剂外用乳膏(主要成分为磷酸芦可替尼)。该药物通过外用途径作用于皮损局部,系统性暴露量低,在保证疗效的同时具有良好的安全性特征。磷酸芦可替尼乳膏已于2026年1月获得中国国家药品监督管理局(NMPA)正式批准上市,用于治疗12岁及以上伴面部受累的非节段型白癜风患者,成为国内率先获批用于白癜风治疗的JAK抑制剂外用制剂。

本次临床研究的主要目的包括:
有效性评估:评估JAK抑制剂外用乳膏治疗非节段型白癜风24周及52周时,面部及全身皮损复色的改善程度,主要观察指标为面部白癜风面积评分指数(F-VASI)较基线的变化率,以及达到F-VASI 50、F-VASI 75(即面部白斑面积改善50%、75%以上)的患者比例;
安全性评估:观察研究药物在真实世界临床应用中,不同年龄段、不同病程、不同皮损部位患者中的安全性特征,包括不良事件发生率、局部耐受性及实验室指标变化;
生活质量影响评估:通过标准化生活质量问卷(如DLQI、Skindex-16等),评估治疗后患者心理状态、社交功能及生活质量的改善情况;
长期疗效观察:通过延长随访期,观察达到复色效果的受试者在停药后色素维持情况,为临床制定个体化治疗方案提供数据支持。
本研究的开展,将为中国白癜风患者提供更多的循证医学证据,进一步验证JAK抑制剂外用制剂在中国人群中的疗效和安全性特征,为优化临床治疗策略、实现精准治疗奠定基础。
入选标准
如果您或您的亲友符合以下基本条件,可能有机会参与本次研究:
• 年龄要求:年龄≥12周岁,性别不限;
• 诊断标准:临床确诊为非节段型白癜风(包括进展期或稳定期);
• 全身受累体表面积(BSA)介于10%以内;
• 面部受累BSA≥0.5%,且面部白癜风面积评分指数(F-VASI)≥0.5;
• 治疗意愿:自愿停止使用可能影响研究结果的其他白癜风治疗方案(以医生制定的治疗方案为准),并同意在整个研究期间仅使用研究指定的治疗方案;
• 知情同意:充分了解本研究内容,自愿签署书面知情同意书,并能配合完成定期的随访和检查。
排除标准
具有以下任一情况者,不宜参加本研究:
• 诊断为节段型白癜风或其他非节段型白癜风以外的色素减退性疾病(如无色素性痣、炎症后色素减退等);
• 筛选期存在活动性炎症性皮肤病(如湿疹、银屑病等),经研究者判断可能干扰疗效评估;
• 既往使用过皮肤脱色剂治疗;
• 伴有进展性或未控制的严重系统性疾病(如心脑血管疾病、恶性肿瘤、严重感染、免疫缺陷等);
• 妊娠期、哺乳期女性,或研究期间有生育计划且不愿采取高效避孕措施者;
• 已知对研究药物或其辅料成分过敏。
可能的风险与受益
潜在受益:参加本研究的受试者,有可能从治疗中获得皮损复色的效果。根据境外III期临床研究及中国真实世界数据,每日两次使用研究药物治疗24周后,有相当比例的患者面部白斑面积获得显著改善,且随治疗时间延长,复色效果持续改善。
潜在风险:研究药物可能引起局部不良反应,如用药部位的痤疮、瘙痒、红斑或刺激感。在已完成的临床试验中,不良反应的严重程度大部分均为1级或2级,未发生与药物相关的严重不良事件(SAE)报告。研究期间,您的病情将由专业医疗团队密切监测,一旦出现不适,将及时得到处理。
其他权益:
01 您将获得免费体检;
02 您将获得相应的医疗补助;
03 您的个人信息是保密的,您的权益将会得到保障。
报名方式
本研究计划招募100名受试者。
如果您符合上述条件,并希望了解更多信息,请通过以下方式联系我们:
招募专线:15170099064
招募期限:即日起至招满为止。
特别提示:本信息发布目的为招募临床试验受试者,不构成任何用药建议或广告宣传。是否入选将由研究医生根据详细的入选/排除标准评估后确定。
附:客观数据支撑
国际III期研究(TRuE-V1/V2):治疗24周时,面部白斑面积改善≥75%(F-VASI 75)的患者比例达到29.9%(安慰剂组为7.5%-12.9%)。
中国真实世界研究:使用24周后,达到F-VASI 75的患者比例为49.5%,疗效积极。
安全性数据:长期使用至52周,未发现新的安全性事件。
TAG:
相关阅读
- 2026-04-26南昌去哪治白癜风医院好-热点聚焦:南昌白癜风医院排行榜
- 2026-04-26南昌白癜风治疗专业的医院-「医疗资讯」南昌白癜风医院排名总榜“排名公布”
- 2026-04-25南昌治白癜风哪家医院好-官方宣布:南昌白癜风的医院排名[实时更新]
- 2026-04-25南昌白癜风哪个医院好-南昌专治白癜风医院排名公开
- 2026-04-24南昌看白癜风哪个医院好-公布排名直击!南昌白癜风正规医院
- 2026-04-24南昌治白癜风的专科医院-排名前四:南昌白癜风医院排行总榜发布
推荐阅读
- 南昌看白癜风哪个医院好-公布排名直击!南昌白癜风正规医院
- 南昌治白癜风的专科医院-排名前四:南昌白癜风医院排行总榜发布
- 南昌哪家医院看白癜风好一些-排行榜出炉:南昌白癜风医院排名名单公布
- 南昌治白癜风哪个医院好-网上挂号入口:2026白癜风医院排行榜南昌前4排名公布
- 南昌白癜风能在哪里治-白癜风名单:南昌专业白癜风医院排行总榜公开
- 南昌哪有白癜风专科医院-热点推荐!南昌看白癜风医院排名总榜发布公开宣布
- 南昌治疗白癜风哪个医院好-排名宣布:南昌白癜风医院在哪“引关注”
- 南昌治白癜风的医院哪家好-公开宣布:南昌白癜风医院三大排名榜
- 南昌治疗白癜风哪个医院好-排名宣布:南昌白癜风医院在哪“引关注”
- 南昌治白癜风的医院哪家好-公开宣布:南昌白癜风医院三大排名榜
- 南昌看白癜风的专科医院-白癜风专栏:南昌白癜风医院排名总榜
- 南昌白癜风哪家好-「重大爆料」南昌白癜风医院排名创新高
- 南昌白癜风能在哪里治-白癜风名单:南昌专业白癜风医院排行总榜公开
- 南昌哪有白癜风专科医院-热点推荐!南昌看白癜风医院排名总榜发布公开宣布
- 南昌治疗白癜风哪个医院好-排名宣布:南昌白癜风医院在哪“引关注”
- 南昌治白癜风的医院哪家好-公开宣布:南昌白癜风医院三大排名榜
- 南昌看白癜风的专科医院-白癜风专栏:南昌白癜风医院排名总榜
- 南昌白癜风哪家好-「重大爆料」南昌白癜风医院排名创新高
- 南昌看白癜风好的医院-白癜风名单:南昌专业白癜风医院排行榜总榜公开
- 南昌哪有看白癜风的医院-具体排名:南昌治白癜风排名前四白癜风医院
- 南昌白癜风医院是哪家-排名TOP3:南昌白癜风医院排名前三强公布
- 南昌有没有治疗白癜风专科医院-口碑排名榜:南昌白点癜风医院公开排名总榜
- 南昌哪里有白癜风医院-科普白癜风:南昌有几个白癜风医院三大排名医院
- 南昌有什么医院看白癜风-南昌白癜风医院口碑榜排名前3强公开榜
- 南昌治白癜风的医院在哪里-白癜风名单!南昌白癜风医院排行榜“总榜公开”
- 南昌去哪看白癜风-今日排名:南昌皮肤病白癜风医院排名前三公开
- 南昌哪家医院治白癜风好-口碑排名:南昌白癜风医院十佳排名前三详细名单
- 南昌能看白癜风的医院-重磅宣布:南昌治白癜风医院排名公布
- 南昌白癜风哪家医院好-本月要闻!南昌白癜风医院怎么样热点官宣排名
- 南昌白癜风医院哪儿有-南昌前四名白癜风医院排名总榜
- 南昌白癜风医院排行榜-公开排名:南昌白癜风医院前三强名单
- 南昌什么医院治疗白癜风-公开发布:南昌白癜风医院今日热榜
- 南昌治白癜风的医院哪儿有-焦点反馈!南昌四大白癜风医院排行榜公布
- 南昌哪有白癜风专科医院-南昌四大白癜风医院详细排名公布!
- 南昌看白癜风医院哪个好-南昌白癜风医院排行总榜公布
- 南昌哪家医院冶白癜风好-2026热点南昌白癜风好的医院前三名
- 南昌有治白癜风的吗-2026全新排名:南昌白癜风医院热门排行榜总榜发布
- 南昌治疗白癜风哪个医院疗效好-南昌白癜风医院人气排行榜“前三”
- 南昌看白癜风效果好的医院-焦点排名:南昌三大白癜风医院口碑排行榜公布
- 南昌有没有看白癜风好的医院-白癜风专栏:南昌市白癜风医院具体名单
- 南昌哪里治白癜风专业-排名前三:南昌白癜风医院排行总榜发布技术强
- 南昌有白癜风专科没-南昌医院治疗白癜风排名优先推荐!
- 南昌看白癜风好的医院-白癜风名单:南昌专业白癜风医院排行榜总榜公开
- 南昌哪有看白癜风的医院-具体排名:南昌治白癜风排名前四白癜风医院
- 南昌白癜风医院是哪家-排名TOP3:南昌白癜风医院排名前三强公布
- 南昌有没有治疗白癜风专科医院-口碑排名榜:南昌白点癜风医院公开排名总榜
- 南昌哪里有白癜风医院-科普白癜风:南昌有几个白癜风医院三大排名医院
- 南昌有什么医院看白癜风-南昌白癜风医院口碑榜排名前3强公开榜
- 南昌治白癜风的医院在哪里-白癜风名单!南昌白癜风医院排行榜“总榜公开”
- 南昌去哪看白癜风-今日排名:南昌皮肤病白癜风医院排名前三公开
- 南昌哪家医院治白癜风好-口碑排名:南昌白癜风医院十佳排名前三详细名单
- 南昌能看白癜风的医院-重磅宣布:南昌治白癜风医院排名公布
- 南昌白癜风哪家医院好-本月要闻!南昌白癜风医院怎么样热点官宣排名
- 南昌白癜风医院哪儿有-南昌前四名白癜风医院排名总榜
- 南昌白癜风医院排行榜-公开排名:南昌白癜风医院前三强名单
- 南昌什么医院治疗白癜风-公开发布:南昌白癜风医院今日热榜
- 南昌治白癜风的医院哪儿有-焦点反馈!南昌四大白癜风医院排行榜公布
- 南昌哪有白癜风专科医院-南昌四大白癜风医院详细排名公布!
- 南昌看白癜风医院哪个好-南昌白癜风医院排行总榜公布
- 南昌哪家医院冶白癜风好-2026热点南昌白癜风好的医院前三名
- 南昌有治白癜风的吗-2026全新排名:南昌白癜风医院热门排行榜总榜发布
- 南昌治疗白癜风哪个医院疗效好-南昌白癜风医院人气排行榜“前三”
- 南昌看白癜风效果好的医院-焦点排名:南昌三大白癜风医院口碑排行榜公布
- 南昌有没有看白癜风好的医院-白癜风专栏:南昌市白癜风医院具体名单
- 南昌哪里治白癜风专业-排名前三:南昌白癜风医院排行总榜发布技术强
- 南昌有白癜风专科没-南昌医院治疗白癜风排名优先推荐!
- 南昌医治白癜风效果好的医院-焦点更新!南昌能治疗白癜风的医院排行榜
- 南昌看白癜风哪个医院好-医线观察:南昌看白癜风医院排行榜单排名三大医院
- 南昌哪有瞧白癜风的医院-热搜关注南昌白癜风医院排行榜发布
- 南昌白癜风治疗专科医院-官方公开:南昌白癜风医院排名总榜
- 南昌白癜风医院专家预约-排名快讯:南昌市白癜风医院今日公开
- 南昌哪里治白癜风便宜-南昌白癜风医院排名总榜公开透明
- 南昌哪有诊治白癜风的医院-南昌白癜风医院榜今日发表总榜宣布
- 南昌去哪里能看白癜风-公开就医:南昌白癜风医院排名总榜实时资讯
- 南昌治疗白癜风好的医院-top3排名一览:南昌市白癜风医院评价如何排名直击
- 南昌白癜风医院哪个好-实时揭秘:南昌白癜风医院排行榜总榜发布
- 南昌白癜风治疗专业的医院-2026公开南昌白癜风医院人气排名总榜排名一览
- 南昌白癜风哪家好-排名前四南昌治疗白癜风医院排行榜总榜发布公开推荐
- 南昌白癜风医院哪里好-南昌白癜风医院排名前四名单公开发表
- 南昌哪里有治疗白癜风的医院-口碑排名:南昌治疗白癜风的地方公开透明}
- 南昌哪里有治疗白癜风的医院-南昌专业治疗白癜风医院排名总榜实时公开
- 南昌治白癜风的哪个医院好-TOP4排名一览:南昌白癜风排名好的医院要闻直击



![南昌治白癜风哪家医院好-官方宣布:南昌白癜风的医院排名[实时更新]](http://ncbdf.qm120.com/uploads/image/20260425/8ae306aeb62d65233eb02e56d21c33db.png)




